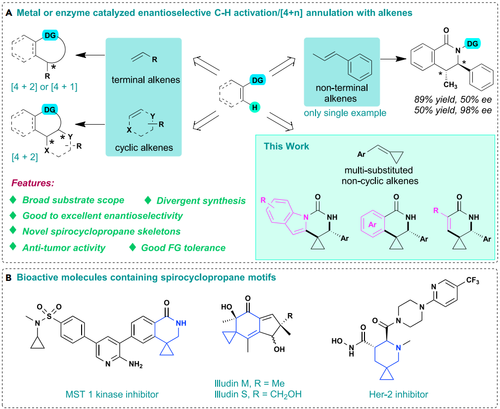
手性螺环一类重要的药物优势骨架,广泛存在于天然产物和药物分子中,具有重要的生物学活性,但如何高效构建这些结构复杂的螺环骨架仍具挑战,也是有机合成领域研究的难点和热点之一。在过去的几十年里,过渡金属催化的不对称C-H活化被认为是构建手性骨架的一种高效而简洁的方法,在报道的反应中通常采用末端烯烃和环烯烃作为重要的合成子来构建复杂的多环骨架,而多取代的非端烯可能由于空间位阻和反应活性低,在不对称C-H活化反应中很少涉及,具有较大挑战性。
中国科学院上海药物研究所周宇课题组和柳红课题组长期致力于螺环骨架化合物库的构建,前期通过过渡金属催化、有机小分子催化等策略实现了多类螺环骨架的构建(Angew.Chem.Int.Ed.2021,60,21327;J.Org.Chem.2016,81,8888;ACS Comb.Sci.2016,18,220;Chem.Commun.2014,50,14771)。在此基础上,该研究团队联合上海药物所/中科中山药物创新研究院吴小伟课题组、丁侃课题组以及广州医科大学易伟课题组于2023年11月27日在Cell Press旗下期刊Chem Catalysis上发表题为“The synthesis of spirocyclopropane skeletons enabled by Rh(III)-catalyzed enantioselective C–H activation/[4+2]annulation”的研究论文。
烯烃的不对称C–H活化进展及新螺环丙烷骨架的构建
在本研究中,团队通过对反应条件的调控,在手性Rh(III)催化剂的作用下实现了芳基酰胺(含吲哚、吡咯、苯、萘、噻吩骨架)、丙烯酰胺与取代非末端烯烃亚甲基环丙烷(MCPs)等底物的不对称C-H活化/[4+2]环合串联反应,高效高对映选择性地实现了多种新颖结构的螺环丙烷骨架的构建。值得一提的是,本研究首次实现了小分子金属催化剂催化丙烯酰胺底物与多取代烯烃底物之间的不对称C-H活化/环化反应。通过药理活性筛选发现化合物(S)-3aj对胰腺癌细胞系BxPC-3具有较好的抗增殖活性(IC50=1.7μM),是潜在的新型结构抗胰腺癌先导化合物。该方法底物适用范围广、反应条件温和,具有优良的收率和对映选择性(up to 98%yield,up to 99.7:0.3 er),为新型螺环丙烷类药物的合成提供了潜在有效的制备方法。
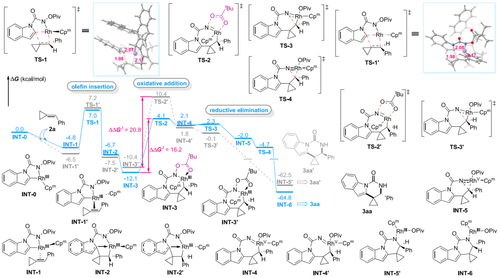
此外,研究团队还通过氢氘(H/D)交换实验、动力学同位素效应(KIE)和密度泛函理论计算(DFT)等研究,对该反应机理进行了详细的探索,解释了手性Rh(III)催化剂如何调控产物对映选择性以及不同酰胺底物的反应性的差别。
手性Rh(III)催化烯烃插入及环化的DFT研究
上海药物所博士研究生王淏、硕士研究生李一迪、南方医科大学硕士研究生黄林、广州医科大学徐慧影博士和上海药物所博士后焦峪坤为该论文共同第一作者。上海药物所周宇研究员、吴小伟副研究员、柳红研究员和广州医科大学易伟教授为该论文的共同通讯作者。上海药物所丁侃研究员在药理活性测试方面给予了支持和指导。本研究还得到了国家自然科学基金、上海浦江人才及广东省科学基金的支持。
全文链接
https://www.cell.com/chem-catalysis/fulltext/S2667-1093(23)00402-5