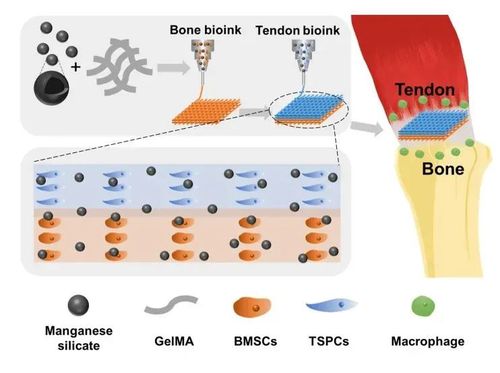
近日,中国科学院上海硅酸盐研究所吴成铁研究员带领的研究团队在免疫多细胞支架用于肌腱-骨修复领域取得重要进展。该团队通过多细胞打印技术将硅酸锰(MS)纳米颗粒与肌腱/骨相关细胞相结合,设计并构建了具有免疫调控功能的多细胞支架,用于肌腱和骨的一体化再生(如图1)。该免疫调节支架不仅在体外展现出多样性的生物活性,而且在多种肩袖损伤(RCT)动物模型中实现了免疫调节、多组织一体化再生和运动功能恢复。
肌腱-骨界面的独特结构可有效缓解应力集中,在人体运动功能中发挥着重要作用。当发生损伤时,由于生理结构复杂和再生能力差,临床手术治疗往往会导致界面处瘢痕组织形成,提高再次损伤几率。传统的生物材料倾向于增强与肌腱-骨直接相关的生物功能,如成骨分化或肌腱分化,但损伤部位三维微环境,尤其是体内免疫细胞引发的炎症反应,同样至关重要。根据研究经验,减少 M1巨噬细胞在肌腱-骨界面的聚集并诱导 M2巨噬细胞极化,可以获得更优的组织学和生物力学特性。但由于界面处的高负荷和高压力,巨噬细胞的 M1 和 M2 在肌腱-骨界面的转化存在延迟,能够导致慢性炎症。因此,开发出兼具多再生活性和免疫调节功能的组织工程支架对于肌腱-骨天然结构恢复至关重要。
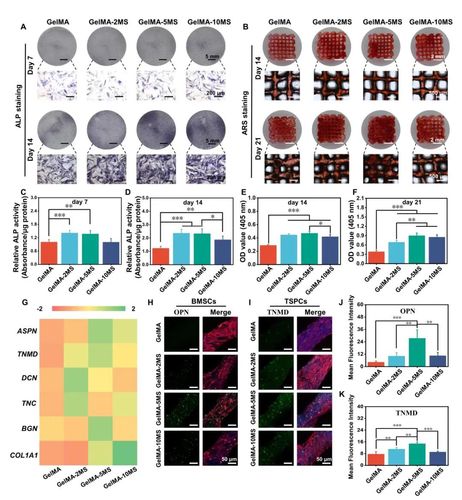
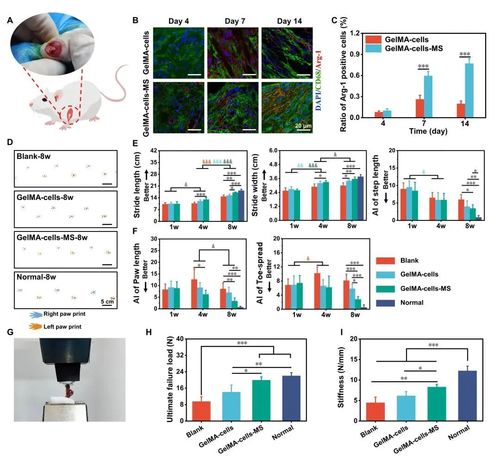
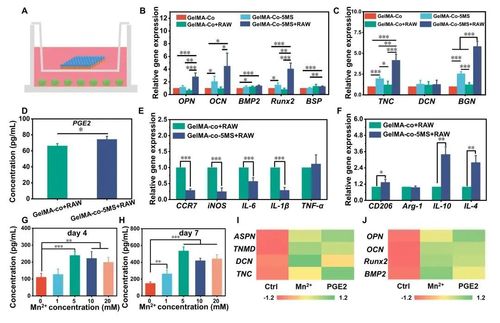
研究团队结合多细胞3D打印技术与硅酸锰(MS)纳米颗粒,构建了免疫多细胞支架,其中肌腱干/祖细胞(TSPCs)和骨髓间充质干细胞(BMSCs)以分层方式分布在支架中,实现了肌腱-骨界面的模拟。得益于多细胞分布和MS纳米颗粒,免疫多细胞支架在体外同时展现了出色的成骨和成肌腱双向分化活性(图2)。此外,多细胞支架在兔和大鼠的RCT模型中同时实现了免疫调节、界面微结构再生和运动功能恢复(图3)。将免疫多细胞支架植入巨噬细胞耗竭的大鼠体内,进一步揭示了免疫调节在多细胞支架的特异性分化中的作用。此外,通过对其免疫生物学机制的探索,免疫多细胞支架能够稳定释放Mn离子刺激巨噬细胞分泌 PGE2,从而增强多细胞的特异性分化(图4)。免疫多细胞支架的构建为软硬组织界面的一体化再生提供了一种前景广阔的新策略。
该研究成果近日发表在Science Advances期刊上(Science Advances, 2024, 10, eadk6610),文章题为“Immunomodulatory Multicellular Scaffolds for Tendon-to-Bone Regeneration”,并申请发明专利一项。论文第一作者为上海硅酸盐所硕士研究生杜琳和博士研究生吴金福,通讯作者为吴成铁研究员。
图1. 基于硅酸锰(MS)纳米颗粒的免疫多细胞支架用于肌腱-骨一体化再生的示意图。